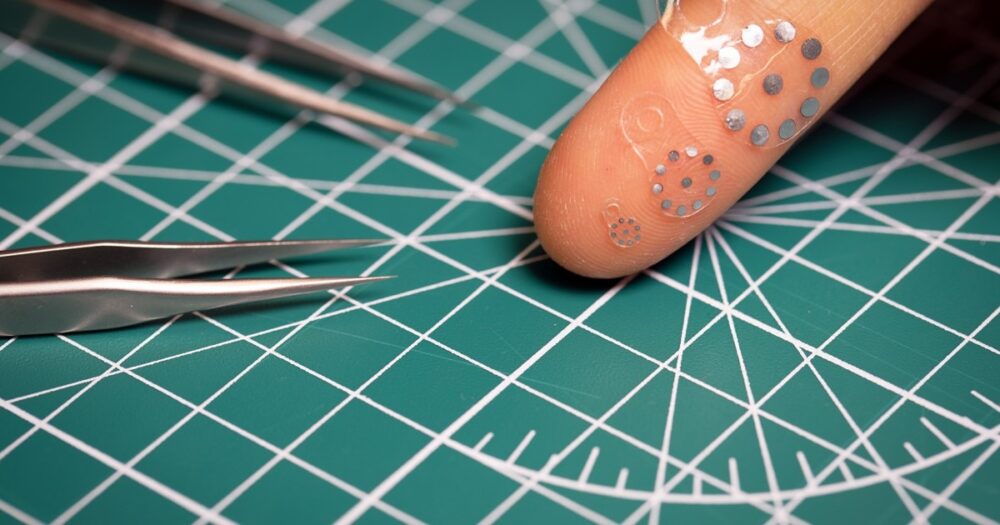
Un team di ricercatori della Northwestern University e dalla Washington University School of Medicine di St. Louis ha messo a punto una nuova tecnologia per il monitoraggio post-chirurgico: degli adesivi idrogel ad ultrasuoni, mutanti e riassorbibili, per il monitoraggio delle perdite anastomotiche. Ma perché mutanti?
Scopriamo l’arcano
Gli adesivi intelligenti
Indice dei contenuti
Quando gli adesivi vengono attaccati a un organo, sono in grado di gonfiarsi in risposta ai sottili cambiamenti nei livelli di pH del corpo. Cambiamenti che possono rivelare i primi segni di complicazioni post-operatorie dopo un intervento del tratto gastrointestinale, come le perdite anastomotiche, che solitamente si verificano tre giorni o due settimane dopo l’intervento.
Le perdite «possono derivare da sottili perforazioni nel tessuto, spesso come spazi impercettibili tra due lati di un’incisione chirurgica» sottolineab John A. Rogers, ideatore del dispositivo.
In aggiunta, se non vengono individuate rapidamente possono portare a gravi conseguenze. Quali? Una probabilità del 30% che il paziente debba rimanere in ospedale per sei mesi ma anche un rischio di morte.
Per coloro che si stanno riprendendo da un intervento chirurgico al pancreas, i rischi sono ancora maggiori. In effetti, tra il 40% e il 60% dei pazienti sperimenta complicazioni dopo questo tipo di intervento.
Problema numero 1: una corsa contro il tempo
Il problema principale è che non è possibile sapere in anticipo chi svilupperà queste complicazioni. Purtroppo, quando i pazienti iniziano a mostrare sintomi, potrebbe essere troppo tardi e potrebbero già essere molto malati.
«Alcuni sintomi associati alla perdita possono essere vaghi», afferma il chirurgo gastrointestinale Chet Hammill. «Ma dopo un grande intervento chirurgico, può essere difficile capire se questi sintomi sono normali o segnali di qualcosa di sbagliato. Se riusciamo a rilevare la perdita in anticipo, possiamo intervenire drenando il fluido. Se invece interveniamo più tardi, il paziente potrebbe sviluppare un’infezione grave e finire in ospedale. Questo è particolarmente critico per i pazienti con cancro al pancreas, poiché potrebbero avere solo sei mesi di vita e trascorrere metà di questo tempo in ospedale».
«La maggior parte delle operazioni all’addome, quando devi rimuovere qualcosa e ricucirlo insieme, comporta il rischio di perdite. Non possiamo prevenire completamente queste complicazioni, ma forse possiamo intervenire prima per ridurre al minimo i danni. Potremmo rilevare una perdita 24 o 48 ore in anticipo e individuare complicazioni prima che il paziente si ammali davvero».
Problema numero 2: la mancanza di strumenti diagnostici
Questi tipi di difetti non possono essere visti direttamente con strumenti di imaging a ultrasuoni. Inoltre sfuggono al rilevamento anche da parte delle scansioni TC e MRI più sofisticate.
«Al momento, non esiste un metodo valido per rilevare questo tipo di perdite», puntualizza Hammill, che ha condotto la valutazione clinica e gli studi su modelli animali alla Washington University, con il collaboratore Dr. Matthew MacEwan, assistente professore di neurochirurgia. Che fare?
Gli adesivi intelligenti
La ricerca di soluzioni innovative per migliorare il benessere dei pazienti ha spinto Hammill a contattare il professor Rogers, pioniere della bioelettronica.
Utile precisare che il team di quest’ultimo ha già sperimentato successi nel campo dei dispositivi elettronici bioriassorbibili, tra cui pacemaker, stimolatori nervosi e antidolorifici impiantabili.
Gli scienziati hanno quindi sviluppato un approccio ingegneristico e una serie di materiali avanzati per rispondere a questa esigenza insoddisfatta nel monitoraggio dei pazienti.
Il professor Rogers ha innanzitutto scelto di utilizzare e trasformare i dispositivi di imaging tradizionali. L’obiettivo era chiaro: “vedere” cose che prima erano invisibili.
Perché trasformarli?
La risposta è semplice. Gli ultrasuoni, scansioni TC e MRI, sebbene siano una risorsa preziosa in medicina, presentano un limite significativo: non riescono a distinguere i vari fluidi corporei. Questo significa che il sangue e i fluidi gastrici appaiono simili, un problema che potrebbe avere conseguenze gravi in ambito chirurgico.
E qui è entrato in gioco l’ingegno del team di Rogers. Perchè non utilizzare dei dispositivi sensoriali ultra piccoli, leggibili attraverso l’imaging ecografico?
La scelta è caduta su degli adesivi mutanti bioriassorbili, realizzati con un materiale chiamato idrogel, flessibile e reattivo chimicamente.
Incorporando minuscoli dischi metallici all’interno di questo idrogel, gli scienziati sono riusciti a ottenere un adesivo che risponde ai fluidi corporei. Quando viene a contatto con fluidi acidi (pH), come quelli dello stomaco, si gonfia. Quando invece incontra fluidi caustici, come quelli pancreatici, si contrae. Quindi, l’ecografia può visualizzare questi sottili cambiamenti nel posizionamento. In che modo?
L’ecografia svela ogni cambiamento
«Poiché le proprietà acustiche dei dischi metallici differiscono notevolmente da quelle del tessuto circostante, creano un contrasto molto evidente nelle immagini ecografiche», chiarisce Rogers. «In pratica, possiamo ‘etichettare’ un organo per monitorarlo in modo accurato».
Ma c’è di più…
Considerando che la necessità di monitoraggio si esaurisce durante il periodo di recupero postoperatorio, il team di Rogers ha sviluppato questi adesivi utilizzando materiali bioriassorbibili.
Veniamo adesso alla scelta dei prototipi.
Gli adesivi al vaglio del studio
In corso d’opera, gli esperti hanno dovuto ovviamente affrontare sfide uniche nel loro percorso. Come creare un adesivo in grado di adattarsi ai cambiamenti di pH del corpo? Come garantire la sensibilità e la specificità necessarie per rilevare le minacce nascoste dei fluidi gastrointestinali?
Il collaboratore computazionale Yonggang Huang, esperto di ingegneria meccanica, ha utilizzato avanzate tecniche di simulazione acustica e meccanica per guidare le scelte ottimizzate nei materiali e nella disposizione dei dispositivi. Cosa che assicura un’elevata visibilità nelle immagini ecografiche, anche per gli adesivi posizionati in profondità nel corpo.
Il team di Rogers ha quindi progettato adesivi di varie dimensioni, dal più grande con un diametro di 12 millimetri al più piccolo con un diametro di soli 4 millimetri. Considerando che i dischi metallici sono estremamente piccoli, ciascuno di 1 millimetro o meno, Rogers aveva tuttavia previsto che la valutazione manuale delle immagini da parte dei radiologi sarebbe potuta essere complicata. Per ovviare a questo problema, il team ha sviluppato un software in grado di analizzare automaticamente le immagini e rilevare con grande precisione qualsiasi cambiamento nella posizione dei dischi.
I test sugli adesivi
Per valutare l’efficacia del nuovo adesivo, il team di Hammill lo ha sperimentato su modelli animali, sia piccoli sia grandi. Negli studi condotti, l’imaging ecografico ha costantemente rilevato cambiamenti nell’adesivo “mutante”, anche quando posizionato a 10 centimetri di profondità nei tessuti.
Risultato?
Se esposto a fluidi con livelli di pH anormalmente alti o bassi, l’adesivo alterava la sua forma in pochi minuti.
Importanza dello studio
Rogers e Hammill ritengono che il dispositivo possa essere impiantato al termine di un intervento chirurgico. Oppure, dato che è piccolo e flessibile, il dispositivo può essere inserito (arrotolato) all’interno di una siringa, che i medici possono utilizzare per iniettarlo nel corpo.
«Questi tag sono così piccoli, sottili e morbidi che i chirurghi possono facilmente posizionarne raccolte in luoghi diversi», chiarisce Rogers. «Per esempio, se un’incisione si estende per pochi centimetri in lunghezza, una serie di questi tag può essere posizionata lungo la lunghezza del sito per sviluppare una mappa del pH e localizzare con precisione la posizione della perdita».
«È ovviamente un prototipo iniziale, ma posso immaginare il prodotto finale in cui, alla fine dell’intervento, si posizionano semplicemente questi piccoli cerotti per il monitoraggio», aggiunge Hammill. «Fa il suo lavoro e poi scompare completamente. Ciò potrebbe avere un impatto enorme sui pazienti, sui loro tempi di recupero e, in definitiva, sulla loro qualità di vita».
In futuro, Rogers e il suo team stanno esplorando tag simili che potrebbero rilevare emorragie interne o cambiamenti di temperatura. «Rilevare i cambiamenti nel pH è un buon punto di partenza»,conclude Rogers. «Ma questa piattaforma può estendersi ad altri tipi di applicazioni mediante l’uso di idrogel che rispondono ad altri cambiamenti nella chimica locale, o alla temperatura o ad altre proprietà di rilevanza clinica».
Fonte
Jiaqi Liu et al, Strutture adattative della forma bioriassorbibili per il monitoraggio ultrasonico dell’omeostasi dei tessuti profondi, Science (2024).
Materiale fornito dalla Northwestern University