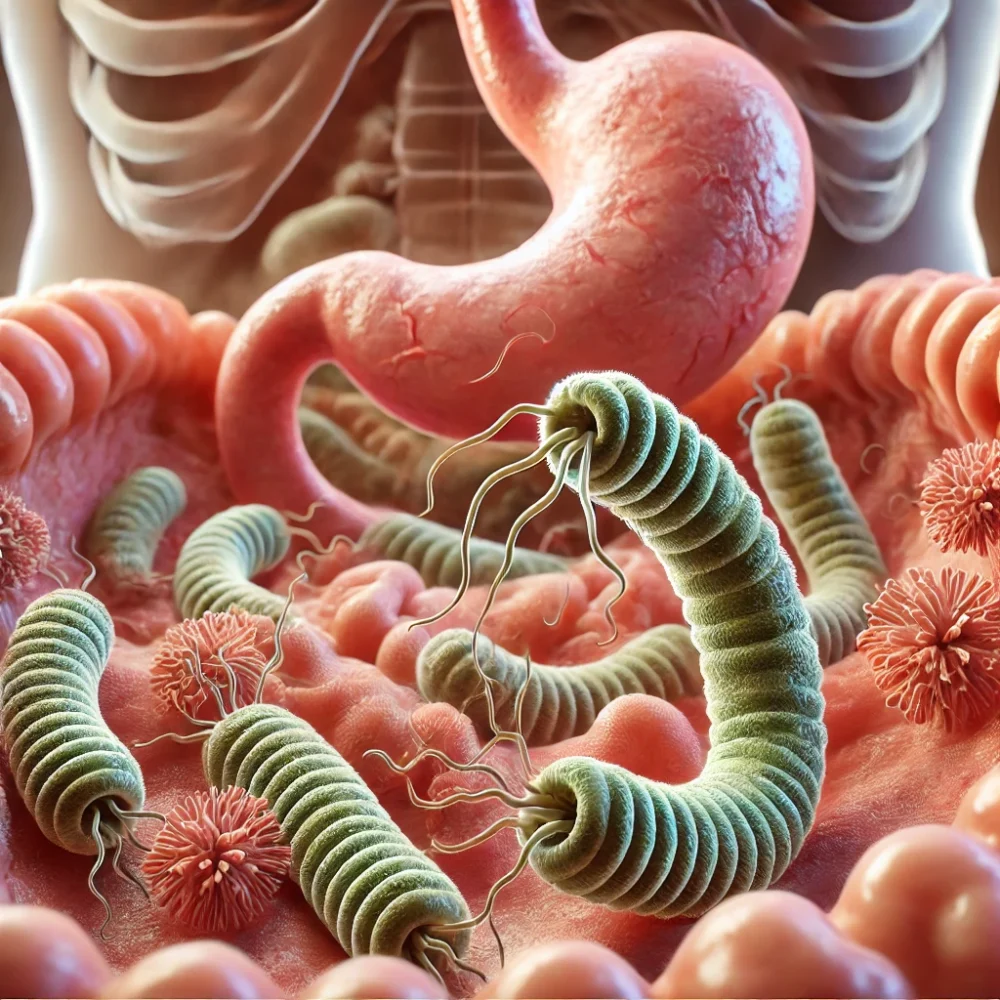
Nel 1982, due scienziati australiani, Barry Marshall e Robin Warren, compirono una scoperta destinata a rivoluzionare la medicina gastroenterologica. Identificarono un batterio a forma di spirale, Helicobacter pylori, capace di sopravvivere nello stomaco umano, un ambiente estremamente acido. Questo microrganismo, dotato di una struttura simile a un cavatappi e di flagelli per muoversi nel muco gastrico, è stato riconosciuto come la causa principale delle ulcere gastriche e, successivamente, di un’importante percentuale di casi di cancro allo stomaco.
Marshall, con un esperimento audace, ingerì il batterio per dimostrarne il legame con la gastrite, guadagnandosi, insieme a Warren, il Premio Nobel per la Medicina nel 2005. Da allora, H. pylori è stato classificato dall’Organizzazione Mondiale della Sanità (OMS) come cancerogeno di classe 1, al pari di agenti noti come il fumo di sigaretta. Oggi sappiamo che circa la metà della popolazione mondiale ospita questo batterio, spesso in modo asintomatico, rendendolo un nemico silenzioso e insidioso
Helicobacter pylori: infezione cronica e rischio di cancro gastrico
Indice dei contenuti
A livello globale, il cancro gastrico, spesso associato all’infezione da Helicobacter pylori, rappresenta una delle principali cause di mortalità oncologica. Con circa 800mila nuovi casi diagnosticati ogni anno, questa forma di adenocarcinoma è particolarmente diffusa in Asia, in Paesi come Giappone, Corea del Sud e Taiwan, dove incidenza e mortalità sono tra le più alte al mondo.
L’infezione cronica da H. pylori provoca infiammazione nello stomaco, portando a gastrite e, nei casi più gravi, a trasformazioni precancerose della mucosa. L’enzima ureasi, prodotto dal batterio, neutralizza l’acido gastrico, creando un ambiente favorevole per la sopravvivenza delle colonie batteriche. Questa persistenza può innescare cambiamenti cellulari che sfociano in tumori maligni.
Nonostante questi rischi, non tutti gli individui infettati sviluppano complicanze. Genetica, dieta ed esposizione ambientale giocano un ruolo cruciale nell’evoluzione dell’infezione verso il cancro. Questa variabilità rende lo screening per H. pylori una sfida complessa ma essenziale per ridurre l’incidenza della malattia.
Lo studio di Taiwan: un passo avanti nello screening di massa
Un recente studio condotto dal National Taiwan University College of Medicine e pubblicato sul Journal of the American Medical Association (JAMA) ha esplorato un approccio innovativo per identificare precocemente i casi di cancro gastrico. Il team, guidato dal dottor Yi-Chia Lee, ha coinvolto oltre 152mila residenti della contea di Changhua, di età compresa tra i 50 e i 69 anni, per valutare l’efficacia di un test combinato che rileva la presenza di H. pylori (HPSA) e il sangue occulto nelle feci (FIT).
Il FIT è comunemente utilizzato per lo screening del cancro al colon, ma ha dimostrato anche una certa efficacia nell’individuare adenocarcinomi dello stomaco. L’aggiunta del test HPSA mirava a migliorare la sensibilità dello screening, offrendo un quadro più completo. I partecipanti sono stati randomizzati in due gruppi: uno sottoposto al test combinato HPSA-FIT e un altro al solo FIT.
I risultati e le difficoltà dello screening
I risultati dello studio hanno evidenziato una lieve riduzione dell’incidenza del cancro gastrico nel gruppo sottoposto al test combinato (0,032%) rispetto al gruppo FIT (0,037%). Tuttavia, la mortalità per cancro gastrico è rimasta invariata tra i due gruppi, sollevando interrogativi sull’efficacia complessiva dello screening aggiuntivo per H. pylori.
Uno dei problemi principali nello screening di massa è la diffusione ubiquitaria di H. pylori. Sebbene la metà della popolazione mondiale sia portatrice del batterio, solo una minoranza sviluppa complicanze significative. Questo dato sottolinea la necessità di criteri di selezione più specifici per individuare le persone a rischio effettivo.
La terapia combinata come arma preventiva
Per i pazienti in cui viene rilevata un’infezione attiva, il trattamento prevede una terapia antibiotica combinata, spesso associata a un inibitore della pompa protonica (PPI) per ridurre l’acidità gastrica. Questa strategia terapeutica, già consolidata per il trattamento delle ulcere peptiche, si è dimostrata efficace nel prevenire l’evoluzione del cancro gastrico. Tuttavia, l’abuso di antibiotici rappresenta una minaccia crescente, poiché può favorire lo sviluppo di resistenze batteriche.
Helicobacter: prevenzione e personalizzazione
La lotta contro H. pylori e il cancro gastrico richiede un approccio multidimensionale. Da un lato, occorre affinare gli strumenti di screening per identificare con precisione i soggetti a rischio. Dall’altro, è fondamentale educare la popolazione sull’importanza della prevenzione, che passa attraverso una dieta equilibrata e l’eliminazione di fattori di rischio, come il fumo e l’abuso di alcol.
Studi come quello condotto a Taiwan rappresentano un passo importante verso una medicina personalizzata, in cui la prevenzione e il trattamento riescono ad adattarsi alle caratteristiche individuali. Sebbene i risultati attuali non abbiano risolto tutte le incognite, offrono spunti preziosi per future ricerche.
Fonti
Yi-Chia Lee et al., “Fecal Immunochemical Test and Helicobacter pylori Stool Antigen Co-Testing,” JAMA
International Agency for Research on Cancer (IARC)
Organizzazione Mondiale della Sanità